通过深度学习解释和研究 Covid-19 X 射线分类器
关键字:深度学习,Grad-CAM,X 射线,Covid-19,HealthShare,IRIS
目的
在复活节周末,我谈到了一些针对 Covid-19 肺的深度学习分类器。 演示结果还算不错,似乎与当时有关该主题的一些学术研究刊物相吻合。 但它真的足够“好”吗?
最近,我偶然收听了一个关于“机器学习中的可解释性”的在线午餐网络讲座,Don 在演讲的最后谈到了这个分类结果:

上图也出现在 “Why Should I Trust You?” Explaining the Predictions of Any Classifier 这篇研究论文中。 我们可以看到,分类器实际上经过训练,以背景像素(如雪等野生环境)作为主要输入,对宠物狗和野狼进行分类。
这关乎我过去的兴趣,现在也激起一些好奇:
- 我们如何“观察”这些通常以“黑盒”形式表示的 Covid-19 分类器,了解哪些像素实际上促成了“Covid-19 肺”结果?
- 在这种情况下,我们可以利用的最简单的形式或工具是什么?
这也是篇简单的 10 分钟笔记。 最后,我会谈到为什么它也与我们即将推出的全新 IRIS 和 HealthShare 功能有关。
范围
幸运的是,过去几年中,各种 CNN 衍生分类器都有了方便的工具:
- CAM(类激活图):其应用在这里和这里得到了充分解释。
- Grad-CAM(梯度加权类激活):这是 CAM 更通用的版本,让我们能够观察整个模型中的任何 CNN 层。
我们将使用 Grad-CAM 对我们上一篇帖子中的 Covid-19 肺分类器进行快速演示。
"Tensorflow 2.2.0rc + Jupyter" Docker 在配备 Nvidia T4 GPU 的 AWS Ubuntu 16.04 服务器上使用。 TensorFlow 2 提供了简单的梯度带实现。
这是我在 Ubuntu 服务器上启动的快速笔记:
docker run -itd --runtime=nvidia -v /zhong/tf/:/tf -p 8896:8888 -p 6026:6006 --name tf-gpu2 tensorflow/tensorflow:2.2.0rc2-gpu-py3-jupyter
方法
您可以放心地在此处忽略以上 Grad-CAM 研究出版物中引用的数字。
这里引用这些数字只是为了对后面使用的 Python 代码进行连续的原始提案(第 4 页和第 5 页)交叉检查,也希望能提供更好的结果透明度。
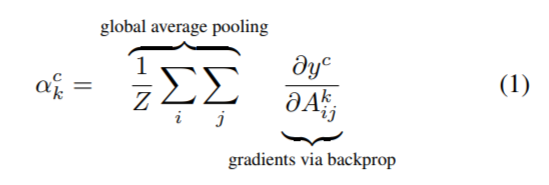
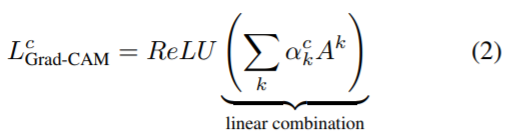
(1):为了得到任意类 c 的宽度 u 和高度 v 的类判别定位图,我们首先计算类 c 的得分相对于卷积层的特征图 Ak 的梯度 yc(softmax 前)。 这些回流的梯度被全局平均池化,得到目标类的神经元重要性权重 ak。
(2):计算出目标类 c 的 ak 后,我们对激活图进行加权组合,然后执行 ReLU。 这就得到了与卷积特征图大小相同的粗略热图。
测试
现在,我们来尝试一下目前能找到的最简单的编码:
1. 导入软件包
import tensorflow as tf;
print(tf.version)
2.2.0-rc2
import tensorflow as tf
import tensorflow.keras.backend as K
from tensorflow.keras.applications.inception_v3 import InceptionV3
from tensorflow.keras.preprocessing import image
from tensorflow.keras.applications.inception_v3 import preprocess_input, decode_predictions
import numpy as np
import os
import imutils
import matplotlib.pyplot as plt
import cv2
2. 加载我们之前训练和保存的模型
new_model = tf.keras.models.load_model('saved_model/inceptionV3')<br>new_model.summary()

可以看到,在最终的全局平均池化之前,模型中 4D 的最后一个 CNN 层被称为“mixed10”。
3. 计算 Grad-CAM 热图
下面是一个实现了上述 Grad-CAM 公式 (1) 和 (2) 的简单版本热图。 这篇帖子对其做出了解释。
with tf.GradientTape() as tape:<br> last_conv_layer = model.get_layer('mixed10') <br> iterate = tf.keras.models.Model([model.inputs], [model.output, last_conv_layer.output])<br> model_out, last_conv_layer = iterate(testX)<br> class_out = model_out[:, np.argmax(model_out[0])]<br> grads = tape.gradient(class_out, last_conv_layer)<br> pooled_grads = K.mean(grads, axis=(0, 1, 2)) heatmap = tf.reduce_mean(tf.multiply(pooled_grads, last_conv_layer), axis=-1)
在我们的示例中,它将生成一个热图 NumPy 数组 (27, 6, 6)。 然后,我们可以将它重新调整为原始 X 射线图像尺寸并叠加在 X 射线图像上方。
不过,在这种情况下,我们将使用略详细的版本,这篇帖子对此也有很好的解释。 它组成了一个函数,Grad-CAM 热图已调整为原始 X 射线图的大小:
# import the necessary packages<br>from tensorflow.keras.models import Model<br>import tensorflow as tf<br>import numpy as np<br>import cv2
class GradCAM:<br> def init(self, model, classIdx, layerName=None):<br> self.model = model<br> self.classIdx = classIdx<br> self.layerName = layerName<br> if self.layerName is None:<br> self.layerName = self.find_target_layer()
def find_target_layer(self):<br> for layer in reversed(self.model.layers):<br> # check to see if the layer has a 4D output<br> if len(layer.output_shape) == 4:<br> return layer.name raise ValueError("Could not find 4D layer. Cannot apply GradCAM.")
def compute_heatmap(self, image, eps=1e-8):<br> gradModel = Model(<br> inputs=[self.model.inputs],<br> outputs=[self.model.get_layer(self.layerName).output,<br> self.model.output]) # record operations for automatic differentiation<br><strong> with tf.GradientTape() as tape:<br> inputs = tf.cast(image, tf.float32)<br> (convOutputs, predictions) = gradModel(inputs)<br> loss = predictions[:, self.classIdx]</strong> # use automatic differentiation to compute the gradients<br> grads = tape.gradient(loss, convOutputs) # compute the guided gradients<br> castConvOutputs = tf.cast(convOutputs > 0, "float32")<br> castGrads = tf.cast(grads > 0, "float32")<br> guidedGrads = castConvOutputs * castGrads * grads convOutputs = convOutputs[0]<br> guidedGrads = guidedGrads[0] weights = tf.reduce_mean(guidedGrads, axis=(0, 1))<br> cam = tf.reduce_sum(tf.multiply(weights, convOutputs), axis=-1)
# resize the heatmap to oringnal X-Ray image size<br> (w, h) = (image.shape[2], image.shape[1])<br> heatmap = cv2.resize(cam.numpy(), (w, h))
# normalize the heatmap<br> numer = heatmap - np.min(heatmap)<br> denom = (heatmap.max() - heatmap.min()) + eps<br> heatmap = numer / denom<br> heatmap = (heatmap * 255).astype("uint8")
# return the resulting heatmap to the calling function<br> return heatmap
4. 加载 Covid-19 肺部 X 射线图
现在,加载一个从未在模型训练和验证过程中使用过的测试 X 射线图。 (也已上传到上一篇帖子中)
filename = './test/nejmoa2001191_f1-PA.jpeg'
orignal = cv2.imread(filename)
plt.imshow(orignal)
plt.show()

调整为 256 x 256,归一化为像素值在 0.0 到 1.0 之间的 numpy 数组“dataXG”。
orig = cv2.cvtColor(orignal, cv2.COLOR_BGR2RGB)<br>resized = cv2.resize(orig, (256, 256))<br>dataXG = np.array(resized) / 255.0<br>dataXG = np.expand_dims(dataXG, axis=0)
**5. 进行快速分类 **
现在可以调用上面新加载的模型进行快速预测:
preds = new_model.predict(dataXG)<br>i = np.argmax(preds[0])<br>print(i, preds)
0 [[0.9171522 0.06534185 0.01750595]]
因此它被归类为 0 型 - Covid-19 肺,概率为 0.9171522。
6. 计算 Grad-CAM 热图
# Compute the heatmap based on step 3<br>cam = GradCAM(model=new_model, classIdx=i, layerName='mixed10') # find the last 4d shape "mixed10" in this case<br>heatmap = cam.compute_heatmap(dataXG)
#show the calculated heatmap
plt.imshow(heatmap)
plt.show()

7. 在原始 X 射线图上显示热图
# Old fashioned way to overlay a transparent heatmap onto original image, the same as above<br>heatmapY = cv2.resize(heatmap, (orig.shape[1], orig.shape[0]))<br>heatmapY = cv2.applyColorMap(heatmapY, cv2.COLORMAP_HOT) # COLORMAP_JET, COLORMAP_VIRIDIS, COLORMAP_HOT<br>imageY = cv2.addWeighted(heatmapY, 0.5, orignal, 1.0, 0)<br>print(heatmapY.shape, orig.shape)
# draw the orignal x-ray, the heatmap, and the overlay together<br>output = np.hstack([orig, heatmapY, imageY])<br>fig, ax = plt.subplots(figsize=(20, 18))<br>ax.imshow(np.random.rand(1, 99), interpolation='nearest')<br>plt.imshow(output)<br>plt.show()
(842, 1090, 3) (842, 1090, 3)
 这似乎表明我们的 Covid-19 演示分类器“相信”患者的“右侧气管旁带”周围出现了一些“浑浊”问题? 我不是很明白,这要请教真正的放射科医生。
这似乎表明我们的 Covid-19 演示分类器“相信”患者的“右侧气管旁带”周围出现了一些“浑浊”问题? 我不是很明白,这要请教真正的放射科医生。
那么,接下来再尝试一些从现实世界案例提交到 GitHub 仓库中的测试图像:
filename = './test/1-s2.0-S0929664620300449-gr2_lrg-b.jpg'
0 [[9.9799889e-01 3.8319459e-04 1.6178709e-03]]
这似乎也是合理的 Covid-19 解释,表明问题更多地发生在左心线区域?

再试试另一个随机测试 X 射线图:
filename = '../Covid_M/all/test/covid/radiol.2020200490.fig3.jpeg'
0 [[0.9317619 0.0169084 0.05132957]]
没想到这并不完全正确,但看起来好像也不算太离谱? 它显示了两个问题区域,左侧为主要问题,右侧为部分问题,这与放射科医师的标记应该是有些对应的? (希望它不是在人类标记上训练 - 这是可解释性问题的另一个层面)。
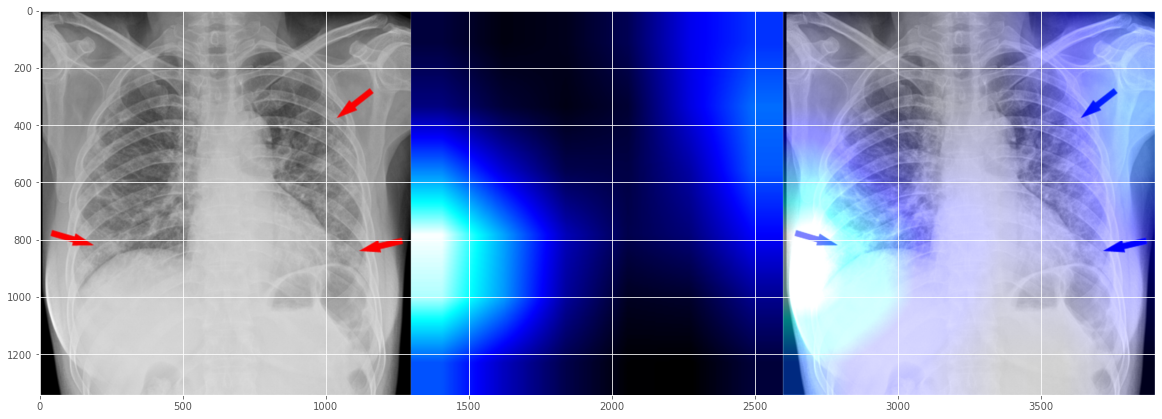
我要在这里打住了,我猜不会有太多人对 X 射线感兴趣。
原因
我个人对“可解释性”和“可理解性”以及相关技术方法的重要性有着深切的体会。 在此领域的任何尝试都是值得的,无论它有多么微不足道。 最终,“数据公平”、“数据公正”和“数据信任”将建立在其数字经济过程透明化的基础之上。 另外,它现在开始能为人所用了。 25 年前,当年轻的我在 1995 年的夏天忙着写博士论文的时候,我甚至不指望对被广泛用作黑盒的所谓“神经网络”有任何了解。 当时的 AI 更像是逻辑推理机“专家系统”,“神经网络”只是被称为“神经网络”,而“深度学习”尚未诞生。 现在,越来越多的研究和工具不断涌现,可供 AI 开发者轻松使用。
最后,具体到这个演示,我很欣赏这种工具的一点是,它甚至不需要以像素级的标记作为起点,而是试图自动生成肺部病变区域,实现一种类似半自动标记的效果。 这在实际应用中是有意义的。 我记得去年,我的一位放射科医生朋友为了帮助我获取一些骨折数据,一遍又一遍地生成 U-Net 训练的像素标签,这很伤眼睛。
未来计划
回到正题。 得益于过去 10 多年深度学习的快速发展,医学影像已成为 AI 领域比较成熟的方向。 这是值得我们深入研究的。 不过,接下来如果有时间,我希望我们能在 NLP 方面多做一些尝试。
致谢
所有来源均已根据需要插入上述文本。 如有其他需要,我还将提供更多引用。
免责声明:
再次说明,我现在写这篇快速笔记是为了防止相关信息随时间遗失。 本文完全是出自“开发者”角度的个人观点。 内容和文本随时可能会被更改或完善。 以上内容主要是展示技术思想和方法,而不是临床解释。临床解释需要放射科专家根据大量优质数据建立黄金规则。